ニュースリリースは報道関係者を対象とした、配信時当時の情報を掲載しています。
医療関係者や一般の方々を対象とした医学的な情報提供や、プロモーションを目的としたものではありません。
報道参考資料
この資料は、インスメッド(米国 ニュージャージー州)が2026年2月19日(現地時間)に発表した内容を日本語に翻訳(要約)したもので、参考資料として提供するものです。資料の内容および解釈については、米国における規制等に基づくもの及び英語による記載が優先されます。英語版および関連財務表は、https://insmed.comをご参照下さい。
インスメッド®、2025年第4四半期および通期の業績、
ならびにビジネスアップデート発表
- BRINSUPRI®(ブレンソカチブ)の2026年通年の売上高は少なくとも10億ドルと予想。アリケイス®(アミカシンリポソーム吸入用懸濁液)*の2026年通年の売上高予想は4億5,000万ドルから4億7,000万ドルと改めて発表。
- 2025年通年の売上高は6億640万ドル。
- BRINSUPRIの2025年第4四半期の売上高は1億4,460万ドル、2025年通年では1億7,270万ドル。
- アリケイスの2025年第4四半期の売上高は1億1,920万ドル、2025年通年では4億3,380万ドルで、年間成長19%を反映し、2025年通年ガイダンスの上限を超過。
- 第III相試験(ENCORE試験)と第IIb相試験(CEDAR試験)のトップラインデータの公表は予定通り。
- 肺動脈性肺高血圧症(PAH)の治療薬Treprostinil PalmitilをFDAが希少疾病用医薬品に指定。
- 2025年末時点で約14億ドルの現金、現金同等物、および市場性のある有価証券を保有。
*日本ではアリケイス吸入液590 mg(アミカシン硫酸塩 吸入用製剤)として承認されています。
2026年2月19日、米国ニュージャージー州発 人を第一に考え、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指すグローバルバイオ医薬品企業のインスメッド(Nasdaq: INSM)は、2025年12月31日に終了した第4四半期および通年の業績、ビジネスアップデートを発表しました。
インスメッド会長兼最高経営責任者(CEO)のウィル・ルイスは、「2025年を締めくくり、インスメッドにとって刺激的な新たな一年を迎えるにあたり、深刻な疾患と生きる患者さんに貢献できる今後の大きな機会に強い意欲を感じています。」と述べたうえで「米国でのBRINSUPRIの上市は当社の期待を上回って推移しており、これまで承認された治療選択肢がなかった患者さんに本剤をお届けできることを誇りに思います。2026年を通じて、気管支拡張症の患者さんにBRINSUPRIを引き続き届けるとともに、TPIPの第III相臨床プログラムを拡大し、さらに初期段階のパイプラインを前進させてまいります。これにより研究開発基盤を強化し、患者さんの人生を変えうる次世代の治療法創出につなげていきたいと考えています。」と述べています。
| 治療領域における主なハイライト |
| 呼吸器系 |
| BRINSUPRI |
| |
- 2026年通期のBRINSUPRIの売上高は少なくとも10億ドルに達する見込みです。
- 2025年11月、欧州委員会は、過去12か月間に2回以上の増悪歴を有する12歳以上の非嚢胞性線維症気管支拡張症(NCFB)患者の治療薬として、BRINSUPRI(ブレンソカチブ、25mg錠)を承認しました。
- NCFBの治療薬としてのブレンソカチブについては、英国および日本においては2026年中に規制当局の判断が下される見込みです。
- 今後の海外における上市時期に影響を及ぼす可能性のある米国の政策動向の変化については、引き続きその影響を評価しています。
|
|
| アリケイス |
| |
- 2026年通期のアリケイスの売上高は、4億5,000万米ドルから4億7,000万米ドルの範囲となる見込みです。
- アリケイスの2025年の売上高は、2024年比で19%増加しました。全地域において前年比で成長を示し、2025年の売上ガイダンスである4億2,000万米ドルから4億3,000万米ドルの上限を上回りました。
- 新規に診断されたまたは再発したマイコバクテリウム・アビウムコンプレックス(MAC)による肺疾患(肺MAC症)で、抗菌薬による治療を開始していない患者を対象とした第III相ENCORE試験のトップラインデータが、2026年3月または4月に公表される見込みです。
- ENCORE試験のトップライン結果が良好であった場合、2026年後半に、すべての肺MAC症患者を対象とする適応拡大に向けた申請(sNDA)を米国食品医薬品局(FDA)に提出する予定です。同様に、日本における適応拡大に向け、2026年後半に医薬品医療機器総合機構(PMDA)とデータの検討を行う予定です。
|
|
| TPIP |
| |
- 2026年1月、FDAの希少疾病用医薬品開発室より、treprostinil palmitilは肺動脈性肺高血圧症(PAH)の治療薬として希少疾病用医薬品指定(ODD)を受けました。2026年前半には、PAH患者を対象としたTPIP(treprostinil palmitil吸入粉末剤)の第III相試験を開始する予定です。
- 間質性肺疾患に伴う肺高血圧症(PH-ILD)患者を対象としたTPIPの第III相試験(PALM-ILD試験)において、患者登録を積極的に進めています。
- 2026年1月にダブリンで開催されたPulmonary Vascular Research Institute(PVRI)2026 Congressにおいて、TPIPプログラムに関する4件の抄録を発表しました。
- PAHを対象としたTPIPの第IIb相試験の非盲検延長試験(OLE)のデータを、2026年後半に報告する見込みです。
- 上記の第III相試験に加えて、進行性肺線維症(PPF)および特発性肺線維症(IPF)患者を対象としたTPIPの第III相試験を、2026年後半に開始する見込みです。
|
|
| INS1148 |
| |
- 2025年12月、幹細胞因子(Stem Cell Factor:SCF)の特定のアイソフォームであるSCF248を標的とする第II相試験開始準備段階のモノクローナル抗体INS1148を取得しました。
- INS1148については、まず間質性肺疾患(ILD)および中等症から重症の喘息を対象として、第II相試験の開発プログラムを推進する予定です。
|
|
| 免疫および炎症
|
| |
- 2025年10月、化膿性汗腺炎(HS)患者を対象としたブレンソカチブの第IIb相CEDAR試験における患者登録を完了しました。CEDAR試験のトップラインデータは、2026年第2四半期に公表する見込みです。
|
|
| INS1033 |
| |
- ジペプチジルペプチダーゼ1(DPP1)阻害薬の2つ目の開発品であるINS1033は、関節リウマチ(RA)および炎症性腸疾患(IBD)を対象として臨床試験に向けて開発を進めており、初回のIND申請は2026年を見込んでいます。
|
|
| 神経およびその他の希少疾患
|
| |
- 髄腔内投与遺伝子治療薬INS1201のデュシェンヌ型筋ジストロフィー(DMD)患者を対象とした第I相試験(ASCEND試験)で、引き続き患者登録を進めています。
|
|
| INS1202 |
| |
- 2026年1月、筋萎縮性側索硬化症(ALS)患者を対象とする髄腔内投与遺伝子治療薬INS1202の第I相試験(ARMOR試験)において、最初の被験者への投与を実施しました。
|
|
| INS1203 |
| |
- 3つ目の遺伝子治療候補であるINS1203は、スターガルト病を対象として臨床試験に向けた準備を進めており、IND申請は2026年を見込んでいます。
|
|
2025年第4四半期および通期の業績について
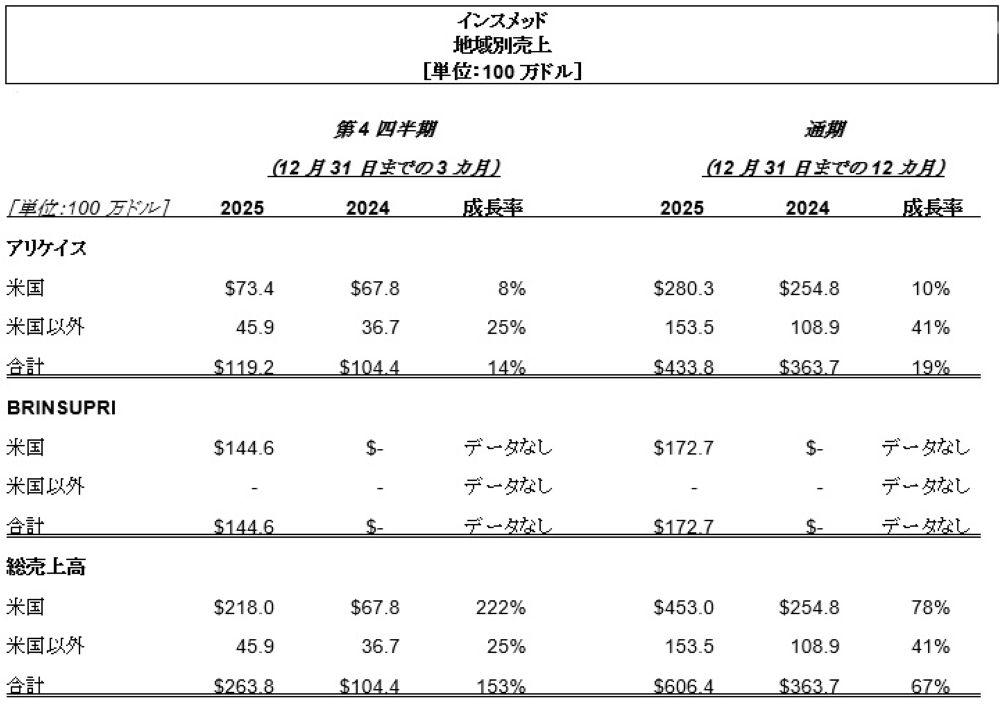
以下の表は、米国、日本、欧州およびその他の地域におけるBRINSUPRIとアリケイスの2025年と2024年の第4四半期および年間売上高と売上成長率をまとめたものです。
| |
- 売上原価(無形資産償却費を除く)は、2025年第4四半期に4,420万ドル、2024年第4四半期は2,620万ドルでした。2025年通年の売上原価(無形資産償却費を除く)は1億2,290万ドルで、2024年通年では8,570万ドルでした。2025年第4四半期および通年における売上原価の増加は、2025年8月のBRINSUPRIの米国での販売開始後、アリケイスおよびBRINSUPRIの売上高の増加を主に反映したものです。売上高に対する売上原価の割合は、アリケイスと比較して製造原価の低いBRINSUPRIの売上増加により、2025年第4四半期および通年において低下しました。
- 研究開発(R&D)費用は、2025年第4四半期に2億5,490万ドル、2024年第4四半期は1億7,970万ドルでした。2025年通年のR&D費用は7億7,110万ドルで、2024年通年は5億9,840万ドルでした。2025年第4四半期および通年におけるR&D費用の増加は、主に人員増に伴う報酬および福利厚生関連費用ならびに株式報酬費用の増加に加え、製造費用の増加およびINS1148の取得によるものです。
- 2025年第4四半期の販売および一般管理費(SG&A)は、2024年第4四半期の1億4,250万ドルに対し2億1,250万ドルでした。2025年通年のSG&A費用は、2024年通年の4億6,110万ドルに対し7億120万ドルでした。2025年第4四半期および通年におけるSG&A費用の増加は、主にBRINSUPRIの販売活動および上市準備及び販売活動に伴う人員増加により、報酬および福利厚生関連費用ならびに株式報酬費用が増加したこと、ならびに専門家報酬およびその他の外部費用の増加によるものです。
- 2025年第4四半期において、インスメッドは純損失3億2,850万ドル(1株あたり1.54ドル)を報告しました。2024年第4四半期の純損失は2億3,550万ドル(1株あたり1.32ドル)でした。2025年通年において、インスメッドは純損失12億7,680万ドル(1株あたり6.42ドル)を報告しました。2024年通年の純損失は9億1,380万ドル(1株あたり5.57ドル)でした。
|
| 貸借対照表、財政ガイダンス、計画投資について |
| |
- 2025年12月31日現在、インスメッドは、合計で約14億ドルの現金、現金同等物、および市場性のある有価証券を保有しています。
- 2026年通年のBRINSUPRIの売上高は、少なくとも10億ドルとなる見込みです。
- 2026年通年のアリケイスの売上高は、4億5,000万~4億7,000万ドルとなる見込みです。
- 前臨床研究プログラムから、年間平均1~2件のIND申請を行うことを見込んでいます。
- 前臨床研究プログラムに係る費用は、全体の支出の20%未満となることを引き続き見込んでいます。
- 弊社は2026年には以下の主要な活動への投資を計画しています。
- 「BRINSUPRI」および「アリケイス」のグローバルでのさらなる拡大。
- 第III相ENCORE試験のトップライン結果が良好であることを前提として、米国におけるアリケイスの完全承認(full approval)に向けた薬事申請の準備、ならびに米国および日本における肺MAC症の全患者を対象とした適応拡大に向けた必要な薬事手続きの準備。
- TPIPの臨床開発プログラムの推進。PH-ILD、PAH、PPF、およびIPF患者を対象とした第III相試験を含みます。
- ILDおよび中等症から重症の喘息を対象としたINS1148の臨床開発プログラムの推進。
- DMDを対象としたINS1201およびALSを対象としたINS1202の臨床試験の推進、ならびにスターガルト病を対象としたINS1203のIND申請準備活動。
- RAおよびIBDを対象としたINS1033のIND申請に向けた活動の推進。
- 前臨床研究プログラムの継続的開発。
|
|
|
カンファレンスコール
インスメッドは、2026年2月19日午前8時(米国東部時間)よりカンファレンスコールを実施しました。この会議のウェブキャストは、当社ウェブサイト(www.insmed.com)の投資家情報セクションに90日間保存されます。
アリケイスについて
アリケイスは、米国ではARIKAYCE®(Amikacin Liposomal Inhalation Suspension/ALIS, アミカシンリポソーム吸入用懸濁液)、欧州ではARIKAYCE® Liposomal 590 mg Nebuliser Dispersion、日本ではアリケイス®吸入液590 mg(アミカシン硫酸塩 吸入用製剤)として承認されています。現在、国際的な治療ガイドラインでは、適切な患者にアリケイスを使用することが推奨されています。アリケイスは、これまで静脈内投与され、聴覚、平衡感覚、および腎機能に対する重度の毒性を示す抗菌薬であるアミカシンを、1日1回、吸入投与する新規製剤です。当社独自のPULMOVANCE®リポソーム技術により、アミカシンを肺に直接到達させることで、全身の曝露を抑えながら、主要な感染細胞である肺マクロファージに取り込まれることを可能としました。アリケイスは、PARI Pharma GmbH(以下、PARI社)社製のラミラ® ネブライザシステムを使用して1日1回投与されます。
PARI社とラミラ®ネブライザシステムについて
アリケイスは、PARI社が開発した新しい吸入器であるラミラ®ネブライザシステムによって投与されます。ラミラ®は、振動する多孔質膜を介してアリケイスを効率的に噴霧することができる、静かで持ち運び可能なネブライザです。PARI社は、エアロゾルに関する100年の知見に基づき、患者の治療を向上させるための革新的な送達プラットフォームの開発を通じて、吸入治療の進歩に貢献しています。
BRINSUPRI®(ブレンソカチブ)について
BRINSUPRI®(ブレンソカチブ)は、ジペプチジルペプチダーゼ1(DPP1)を可逆的に阻害する、1日1回投与の低分子経口阻害剤です。BRINSUPRI(ブレンソカチブ10mg錠および25mg錠)は、米国において成人および12歳以上の小児の非嚢胞性線維症気管支拡張症(NCFB)の治療薬として適応を取得しています。欧州連合(EU)においては、過去12か月間に2回以上の増悪歴を有する12歳以上のNCFB患者を対象として、BRINSUPRI(ブレンソカチブ25mg錠)が承認されています。ブレンソカチブは、NCFBの慢性気道炎症を引き起こす主要因とされる好中球内の酵素(好中球セリンプロテアーゼ)の活性化を阻害するように設計されています。ブレンソカチブは、その他の好中球を介する疾患である化膿性汗腺炎(hidradenitis suppurativa)における有用性についても現在評価が進められています。
TPIPについて
Treprostinil palmitil inhalation powder(TPIP)は、開発段階にある炭素数16の炭素鎖にエステル結合で結合したトレプロスチニルで構成される、トレプロスチニルのプロドラッグであるトレプロスチニルパルミチルの乾燥粉末製剤です。TPIPは、当社の研究所で最初から開発された、PAH、PH-ILD、その他の希少かつ重篤な肺疾患患者の治療薬としての評価が行われている、将来が非常に期待される高度に差別化されたプロスタノイドです。TPIPは、カプセル製剤であり、吸入器を使用して投与されます。現在、TPIPは開発治験段階にあり、世界中のどの国・地域においても、承認されていません。
INS1148について
INS1148は、呼吸器疾患ならびに免疫・炎症性疾患といった高いアンメット・メディカル・ニーズを有する疾患を対象に、ファースト・イン・クラスとなる可能性のある治療薬として当社が開発を進めている開発段階のモノクローナル抗体です。INS1148は、その新規の作用機序を通じて、Stem Cell Factor(SCF)の特定のアイソフォームであるStem Cell Factor 248(SCF248)を選択的に標的とします。SCF248に結合することで当該アイソフォームのクリアランスを誘導し、c-Kitシグナル伝達の下流にある炎症カスケードのみを遮断する一方で、生体恒常性の維持および組織修復に関わる経路は維持されます。INS1148は開発段階にある治験薬であり、いずれの国・地域においてもいかなる適応症についても承認されていません。
INS1201について
INS1201は、デュシェンヌ型筋ジストロフィー(DMD)の患者に対する治療法として、当社が開発を進めているマイクロジストロフィンを発現するAAV(アデノ随伴ウイルス)遺伝子治療です。本剤は髄腔内投与により単回固定用量(体重非依存)で投与され、骨格筋および心筋の両方を標的とする可能性があります。現在、INS1201は、世界中のどの国・地域においても、承認されていません。
INS1202について
INS1202は、ヒトスーパーオキシドジスムターゼ1(SOD1)遺伝子を標的とする、アデノ随伴ウイルス9型(AAV9)を用いたショートヘアピンRNA(shRNA)コンストラクトです。INS1202は、SOD1変異を有する筋萎縮性側索硬化症(ALS)患者ならびにSOD1変異を有しないALS患者に対する治療薬候補として、当社が開発を進めています。INS1202は、髄腔内に単回の固定用量(体重に基づかない用量)で投与されます。INS1202は開発段階にある治験薬であり、いずれの国・地域においても、いかなる適応症についても承認されていません。
インスメッドについて
人を第一に考えるグローバルバイオ企業であるインスメッドは、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指しています。当社は既承認薬から、中期から後期開発段階にある治験薬、最もニーズの高い患者コミュニティに提供する先進的な創薬まで、多様なポートフォリオを推進しています。インスメッドの最も進んだ段階にあるプログラムは、米国・日本・欧州で承認された慢性的で衰弱しやすい肺疾患の治療をはじめとする肺疾患と炎症性疾患に関するものです。当社の初期段階の研究プログラムは、遺伝子療法、AIを用いたタンパク質工学、タンパク質製造、RNA端末結合、合成救済など、幅広い技術とモダリティを網羅しています。インスメッドは、米国ニュージャージー州ブリッジウォーターに本社を置き、欧州や日本において事業を展開しています。インスメッドはScience誌のトップエンプロイヤーサーベイで5年連続1位に選ばれ、バイオ医薬品産業で優良企業の1つとして認められています。
日本法人概要
会社名 : インスメッド合同会社
設立日 : 2017年12月5日
住所 : 〒100-0014 東京都千代田区永田町2-10-3 東急キャピトルタワー13階
https://insmed.jp/
Insmed®, Insmed logo, インスメッド®, ARIKAYCE® and アリケイス® are registered trademarks of Insmed Incorporated. PARI® is a registered trademark of PARI GmbH. ラミラ® is a registered trademark of PARI Pharma GmbH. All other trademarks referenced herein are the property of their respective owners.
将来予想に関する記述
本プレスリリースには、重大なリスクおよび不確定要素を伴う将来予想に関する記述が含まれております。1995年米国民事証券訴訟改革法に定義されているように「将来予想に関する記述」は、歴史的事実ではない記述であり、多くのリスクや不確定要素を伴っています。本プレスリリース記載の「かもしれない」、「予定する」、「はずである」、「可能性がある」、「だろう」、「期待する」、「計画する」、「見込む」、「信じる」、「見積もる」、「想定する」、「予測する」、「予定する」、「可能性がある」、「継続する」およびその他同様の表現(ならびに将来の事象、条件、状況に言及しているその他の言葉や表現)は、将来予想に関する記述であることを示しています。
本プレスリリースに記載されている将来予想に関する記述は、当社の現時点での予測や見解に基づくものであり、既知および未知のリスク、不確定要素およびその他の要因を伴っています。これらの要因により、当社の実際の業績、実績、成果および特定の事象の発生時期が、将来予想に関する記述で検討、予測、予想または提示されているそれらと大きく異なる可能性があることをご留意ください。これらのリスク、不確定要素およびその他要因には、以下のものが含まれます。米国、欧州、もしくは日本で ARIKAYCE の商業化を継続的に成功させられないこと、または BRINSUPRI の米国もしくは欧州での商業化に成功しないこと、または ARIKAYCE に対する米国、欧州、もしくは日本の承認を維持できないこと、または BRINSUPRI に対する米国もしくは欧州の承認を維持できないこと。FDA から ARIKAYCE の完全な承認 (full approval) を取得できないこと (ARIKAYCE の完全な承認に必要な市販後確認臨床試験を成功裏にまたは適時に完了できないリスクを含む)、または ARIKAYCE の適応症をより広範な患者集団に拡大するための規制当局の承認を取得できないこと。米国、欧州、もしくは日本において当社製品候補に対する規制当局の承認、米国、欧州、および日本以外においてARIKAYCE に対する規制当局の承認(各市場および各用途での Lamira® Nebuliser Systemの個別の規制当局の承認を含む)、もしくは米国および欧州以外においてBRINSUPRIに対する規制当局の承認を取得できないこと、または取得が遅れること。適用される規制当局の承認を得た場合でも、当社製品候補の商業化に成功しないこと、または承認された場合でも、当該製品候補に対して適用される規制当局の承認を維持できないこと。当社販売製品、または承認された場合には当社製品候補に対する、医師、患者、第三者支払者、および医療コミュニティのその他の者による市場受容度の不確実性または変化。当社販売製品、もしくは承認された場合には当社製品候補について政府または第三者支払者から適切な償還を受けられないこと、または維持できないこと、または当社販売製品、もしくは承認された場合には当社製品候補について当社が許容可能な価格を得られないこと、または維持できないこと。当社販売製品および当社製品候補の潜在的市場規模の当社推定値の不正確性、または、医師、予想される患者導入率、予想される治療期間、または予想される患者の服薬遵守率もしくは中止率を特定するために用いたデータの不正確性。当社が製造を委託している第三者が、商業上または臨床上の必要性に応じて十分な量の当社販売製品および当社製品候補を製造できないこと、当社の臨床試験を実施できないこと、または当社の事業に影響を与える契約または法律および規制を遵守できないこと。 Pharmakon Advisors LP が管理する特定のファンドを通じた当社のシニア担保ローンおよび OrbiMed Royalty & Credit Opportunities IV, LP とのロイヤルティファイナンスに関連するリスクおよび不確実性、ならびに、それらから得られる予定の利益(シニア担保ローンおよびロイヤルティファイナンスに関する契約のコベナンツの遵守を当社が維持すること、および当該契約に基づく当社の事業運営への制約の影響を含む)。効果的な直接販売およびマーケティング基盤を構築もしくは維持できないこと、または当社販売製品もしくは将来承認される当社製品候補のいずれかを流通させるためのかかる基盤を提供する第三者と提携できないこと。当社販売製品または当社製品候補について将来の臨床試験を成功裏に実施できないこと、ならびに、試験を実施および完了し、または当社製品候補の規制承認に必要なデータを生成する、または 肺MAC症のより広範な患者集団で ARIKAYCE を使用できるようにするために十分な数の患者を登録または維持できない可能性があること。当社販売製品または当社製品候補に関連する安全性または有効性に関する予期しない懸念の発生。臨床試験が遅延するリスク、医薬品開発中に重篤な副作用が発見されるリスク、または提出されたプロトコルの修正が却下されるリスク。新規遺伝子治療製品の開発、規制当局の承認および商品化の期間および費用を正確に予測できないこと。当社が随時発表または公表する臨床試験の中間データ、トップラインデータ、または予備データが、より多くの患者データが利用可能になるに伴って変化するリスク、または追加データが開示された場合に異なって解釈されるリスク、または盲検化されたデータが非盲検化されたデータの予測に役立たないリスク。競合他社が、特定の適応症向けに当社が開発中の製品と本質的に同一の製品について希少疾病用医薬品の独占権(ODE)を取得するリスク。主要な人員を確保および維持できないこと、または効果的に成長を管理できないこと。買収先の経営統合に成功せず、経営統合に費やす経営陣の時間と注意を適切に管理できないこと。取得した技術、製品、および製品候補が商業的に成功しないリスク。競争が激しく変化し続ける環境に適応できないこと。当社の技術システムがアクセス、アップグレード、もしくは拡張できないこと、または既存の技術を更新し、または新しい技術を開発し、もしくは実装する際に困難が生じること。当社の重要な顧客を維持できないリスク。医療制度に関する法令又はその他の政府の施策が当社の事業に多大な悪影響を及ぼすリスク。自然災害もしくは公衆衛生上の危機等の大災害またはその他の事象による事業上または経済上の混乱。現在および将来の AI および機械学習の使用が成功しないリスク。米国、欧州、日本、および世界的な経済状況の悪化(当社、当社のサプライヤー、第三者サービスプロバイダー、潜在的なパートナーに影響を与える長期のインフレの影響を含む)。高額な費用のかかる知的財産紛争に巻き込まれ、知的財産権を適切に保護できず、または、営業秘密およびその他の専有情報の開示を防ぐことができず、ならびに、かかる問題に関連する訴訟またはその他の手続きに伴う費用が発生するリスク。 PARIおよびAstraZeneca ABとのライセンス契約を含む、当社販売製品もしくは当社製品候補に関連する契約によって当社に課せられる制限またはその他の義務、およびかかる契約に基づく当社の義務を遵守できないこと。製造物責任請求を含む、当社が当事者であるか、または当事者となる可能性のある訴訟から生じる費用および潜在的評判の悪化。サイバーセキュリティ攻撃または問題が発生した場合に当社の事業が重大な混乱に陥るリスク。当社の事業に適用される法律および規制の変更(価格改革、および、当社製品候補の研究、開発、製造において特定の第三者を活用する当社の能力に影響を与える法律を含む)、ならびに、かかる法律および規制を遵守できないこと。営業損失の履歴、および当社が収益性を達成または維持できない可能性。当社の業績および財務状況に影響を与えるのれんの減損費用。当社の既存の負債を返済できないこと、および、将来の資本にアクセスする当社の能力に関する不確実性。適切な規制当局によって承認された追加の第三者製造施設を建設する計画の実行の遅延、および、かかる計画に関連する予期しない費用。
将来予想に関する記述は、その性質上将来発生するまたは発生しない可能性のある事象に関連し、かつ将来発生するまたは発生しない可能性のある状況に依存するため、リスクおよび不確定要素を伴うことから、当社が将来予想に関する記述で示した実績、計画、意図、または予測を実際に達成できない場合があります。当社の事業に影響を及ぼすリスクや不確定要素に関する追加情報については、2025年12月31日を期末とするインスメッド年次報告書(Form 10-K)およびそれ以降に米国証券取引委員会(SEC)に提出している書類に記載されているItem 1A「リスク要因(Risk Factors)」で説明されている要因をご覧ください。
将来予想に関する記述は、あくまでも本プレスリリースの公表日現在における発表であるため、それらに過度に依拠することのないようご注意ください。当社は、法律および米国証券取引委員会(SEC)の規則で特に定められている場合を除き、予測の変化、かかる記述の根拠となる事象、条件、状況の変化、または実際の結果が将来予想に関する記述に記載されたものと異なる可能性に影響を与えうる変化を反映するために、かかる記述を公に更新または修正する義務を負いません。