ニュースリリースは報道関係者を対象とした、配信時当時の情報を掲載しています。
医療関係者や一般の方々を対象とした医学的な情報提供や、プロモーションを目的としたものではありません。
本資料は、インスメッド(米国ニュージャージー州)が2026年3月23日(現地時間)に発表したプレスリリースを日本語に翻訳・編集したものであり、英語原文には含まれていない日本固有の主要評価項目に関する追加データを含んでいます。原文に関する内容および解釈に相違が生じた場合には、英語原文の記載および米国における規制等に基づく内容が優先されます。本資料は、報道関係者各位へ参考資料として提供するもので、医薬品のプロモーションや宣伝・広告を目的とするものではありません。英語版は、https://investor.insmed.com/2026-03-23-Insmed-Announces-Positive-Topline-Results-from-Phase-3b-ENCORE-Study-of-ARIKAYCE-R-Amikacin-Liposome-Inhalation-Suspension-in-Patients-with-MAC-Lung-Diseaseをご参照ください。
インスメッド®、肺MAC症患者を対象とした
アリケイス®(アミカシンリポソーム吸入懸濁液)*の第IIIb相ENCORE試験におけるトップライン結果が良好であったことを発表
- 本試験は、主要評価項目および多重性調整が行われたすべての副次評価項目である喀痰培養陰性化エンドポイントを達成し、呼吸器症状スコアおよび喀痰培養陰性化率において、統計学的に有意かつ臨床的に意義のある改善を示した。
- また、本試験は日本特有の主要評価項目および試験目的を達成し、15カ月時点における日本特有の持続的喀痰培養陰性化率において、対照薬と比較して統計学的に有意な改善を示した。
- インスメッドは2026年後半に、アリケイスに関する補足的医薬品承認申請(sNDA)を米国食品医薬品局(FDA)に提出するとともに、日本においては、添付文書改訂の可能性を裏付けるため、医薬品医療機器総合機構(PMDA)に本データを提出する予定である。
*日本ではアリケイス吸入液590 mg(アミカシン硫酸塩 吸入用製剤)として承認されています。
2026年4月15日、人を第一に考え、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指すグローバルバイオ医薬品企業のインスメッド(Nasdaq: INSM)は、本日、第IIIb相ENCORE試験のトップライン結果が良好であったことを発表しました。本試験では、抗菌薬未治療で新たに肺MAC症と診断された患者を対象に、アリケイス(アミカシンリポソーム吸入懸濁液)と多剤併用療法(アジスロマイシン250 mg+エタンブトール15 mg/kg)を1日1回投与する群と、プラセボと多剤併用療法を1日1回投与する群を比較検討しました。
ENCORE試験における有効性のトップライン結果は以下の通り:
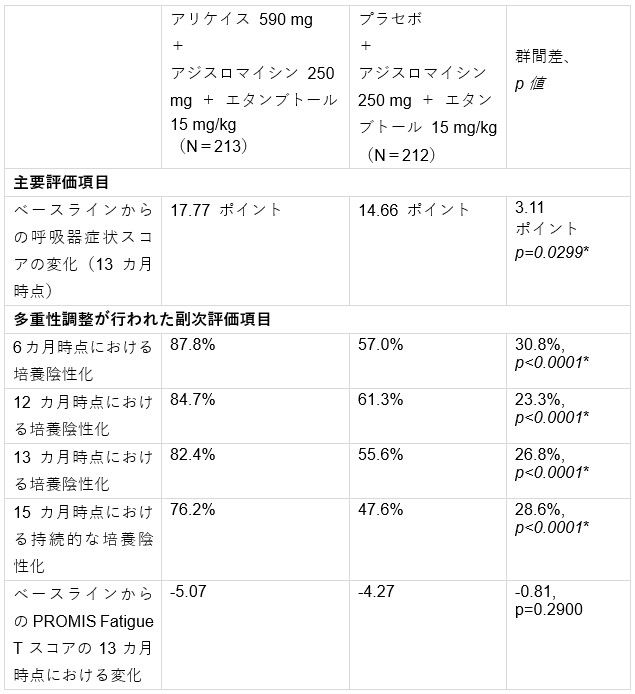
*統計学的に有意
「本結果は、肺MAC症とともに生きる患者さんにとって非常に意義深い成果であり、多剤併用療法の一環としてアリケイスが真の臨床的ベネフィットをもたらすことを力強く裏付けるものです」と、インスメッドの最高医学責任者(CMO)であるマルティナ・フラマー(M.D., M.B.A.)は述べたうえで、「新たに肺MAC症と診断された患者さんが、治療のより早期段階からアリケイスによるベネフィットを得られる可能性に大きな期待を寄せており、米国および日本における本剤の適応拡大の検討を進めていきたいと考えています。最終的には、この困難な疾患と闘うより多くの患者さんの治療成績の向上につなげることを目指しています」と述べています。
本結果により、インスメッドは米国食品医薬品局(FDA)の市販後要件を満たすことを目的とした本試験を完了し、アリケイスを支持する臨床的エビデンスをさらに強化しました。インスメッドは2026年後半に、肺MAC症患者を対象としたアリケイスの補足的新薬承認申請(sNDA)を米国において提出し、適応拡大の可能性を裏付けるとともに、既存の難治例に対する適応について正式承認の取得を目指す予定です。さらに、2026年後半には、日本における適応拡大の可能性を裏付けるため、本データを医薬品医療機器総合機構(PMDA)に提出する予定です。また、これらのデータは今後開催される医学会において発表される予定です。
「今回の画期的な結果は、肺MAC症の治療過程において、より早期から多剤併用療法の一環としてアリケイスを組み入れることで、患者さんに有意な臨床的ベネフィットがもたらされる可能性を示しています」と、National Jewish Health 医学教授であり、ENCORE試験ステアリング委員会メンバーであるDavid Griffith氏(M.D.)は述べたうえで、「呼吸器症状スコアの改善と持続的な喀痰培養陰性化が示されたことは、この重篤でしばしば進行性の感染症に直面する患者さんの治療結果に大きな違いをもたらす可能性を示しています」と述べています。
本試験はまた、日本特有の主要評価項目および試験目的を達成し、15カ月時点における日本特有の持続的喀痰培養陰性化率において、対照薬と比較して統計学的に有意な改善を示しました。
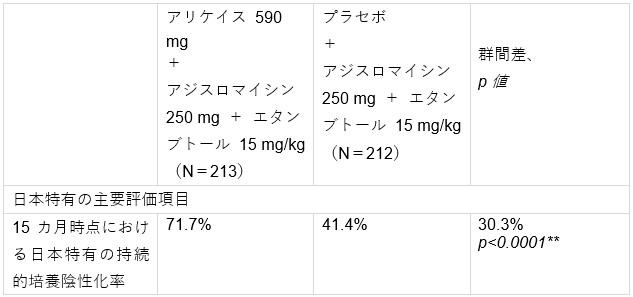
*15カ月時点の日本特有の持続的培養陰性化率の評価項目は、6カ月時点までに培養陰性化を達成し、かつ15カ月時点で持続的培養陰性化を達成した患者の割合
**日本特有の主要評価項目において統計学的に有意
「ENCORE試験の結果は、日本で年々有病率が増加し続けている肺MAC症の患者さんにとって重要な進歩を示しています」と、インスメッド合同会社社長(職務執行者)の中村 誠は述べたうえで、「現在のガイドラインに基づく多剤併用療法にもかかわらず、日本では多くの患者さんが喀痰培養陰性化に至っておらず、より有効な治療選択肢への緊急のニーズが浮き彫りになっています。今回の結果は、アリケイスが意義のある臨床的ベネフィットをもたらすことを改めて裏付けるとともに、治療のより早期段階において役割を果たす可能性を示唆するものです。今後、日本の規制当局と連携し、本剤の適応拡大に向けた検討を進めていきたいと考えており、この困難な疾患に直面するより多くの患者さんの治療の向上に貢献することを目指しています」と述べています。
安全性プロファイルは、アリケイスの既知の安全性プロファイルと一貫しており、新たな安全性シグナルは認められませんでした。治療群において発現率が10%以上であり、かつ対照群と比較してアリケイス群でより高頻度に認められた治療下有害事象(TEAE)は、想定の範囲内でした。全体のTEAEは以下の通りです:
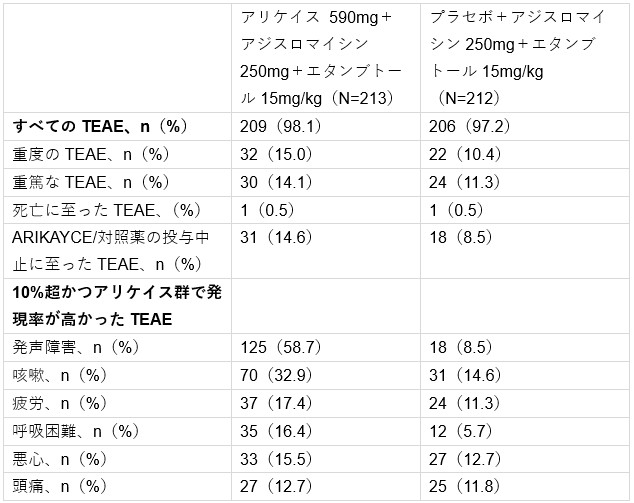
n=少なくとも1件の事象が発生した患者数
特に注目すべきTEAEのうち、気管支痙攣(n=49、23.0% vs n=25、11.8%)および過敏性肺炎(n=5、2.3% vs n=0)は、対照群と比べてアリケイス群でより多くの患者に認められました。一方で、耳毒性(n=55、25.8% vs n=48、22.6%)、基礎肺疾患の増悪(n=23、10.8% vs n=21、9.9%)、喀血(n=22、10.3% vs n=22、10.4%)、神経筋障害(n=5、2.3% vs n=6、2.8%)、および腎毒性(n=1、0.5% vs n=0)については、両群で同程度の発現率でした。死亡例で、アリケイスまたはプラセボとの関連があると判断されたものはありませんでした。治療中止率は、アリケイス群で18.3%、対照群で11.8%でした。試験完了率は、アリケイス群で90.6%、対照群で93.4%でした。
カンファレンスコール
インスメッドは、2026年3月23日午前8時(米国東部時間)よりカンファレンスコールを実施しました。この会議のウェブキャストは、当社ウェブサイト(www.insmed.com)の投資家情報セクションに90日間保存されます。
第IIIb相ENCORE試験について
ENCORE試験は、抗菌薬未治療で新たに肺MAC症と診断された患者を対象に、アリケイスと多剤併用療法の有効性および安全性を評価するために実施された、無作為化、二重盲検、プラセボ対照の第IIIb相試験です。登録患者のうち、82.4%は初回のMAC感染であり、17.6%は2回目または3回目の感染でした。本試験は世界177施設で実施され、合計425例の患者が登録されました。患者は1:1の割合で、アリケイス+多剤併用療法(アジスロマイシン250mg+エタンブトール15mg/kg、n=213)またはプラセボ(吸入用空リポソーム)+多剤併用療法(アジスロマイシン250mg+エタンブトール15mg/kg、n=212)を1日1回、12カ月間投与されました。その後、すべての治験薬投与を中止し、喀痰培養陰性化の持続性を評価するため、さらに3カ月間の追跡が行われました。
主要評価項目は、Quality of Life–Bronchiectasis(QoL-B)の呼吸器領域における8項目に基づく、13カ月時点での呼吸器症状スコアのベースラインからの変化としています。
多重性を考慮した副次評価項目として、6、12および13カ月時点における喀痰培養陰性化達成割合、15カ月時点での持続的喀痰培養陰性化達成割合、ならびに13カ月時点でのPROMIS Fatigue Tスコアのベースラインからの変化を評価しました。日本における主要評価項目は、6カ月時点までの喀痰培養陰性化および15カ月時点での持続的喀痰培養陰性化の両方を達成した患者の割合としています。
肺MAC症について
肺MAC症(Mycobacterium avium complex:MAC)は、罹患率や死亡率を大きく高める可能性のある、まれで重篤な疾患です。肺MAC症の患者は、慢性的な咳、呼吸困難、疲労、発熱、体重減少、胸痛など、時間の経過とともに悪化するさまざまな症状を経験することがあります。また、場合によっては肺に重篤で不可逆的な損傷を引き起こし、致死的となることもあります。肺MAC症は、世界的に公衆衛生上の新たな課題となっており、依然として大きなアンメット・メディカル・ニーズが存在しています。
アリケイスについて
アリケイスは、米国ではARIKAYCE®(Amikacin Liposomal Inhalation Suspension/ALIS, アミカシンリポソーム吸入用懸濁液)、欧州ではARIKAYCE® Liposomal 590 mg Nebuliser Dispersion、日本ではアリケイス®吸入液590 mg(アミカシン硫酸塩 吸入用製剤)として承認されています。現在、国際的な治療ガイドラインでは、適切な患者にアリケイスを使用することが推奨されています。アリケイスは、これまで静脈内投与され、聴覚、平衡感覚、および腎機能に対する重度の毒性を示す抗菌薬であるアミカシンを、1日1回、吸入投与する新規製剤です。当社独自のPULMOVANCE®リポソーム技術により、アミカシンを肺に直接到達させることで、全身の曝露を抑えながら、主要な感染細胞である肺マクロファージに取り込まれることを可能としました。アリケイスは、PARI Pharma GmbH(以下、PARI社)社製のラミラ® ネブライザシステムを使用して1日1回投与されます。
PARI社とラミラ®ネブライザシステムについて
アリケイスは、PARI社が開発した新しい吸入器であるラミラ®ネブライザシステムによって投与されます。ラミラ®は、振動する多孔質膜を介してアリケイスを効率的に噴霧することができる、静かで持ち運び可能なネブライザです。PARI社は、エアロゾルに関する100年の知見に基づき、患者の治療を向上させるための革新的な送達プラットフォームの開発を通じて、吸入治療の進歩に貢献しています。
インスメッドについて
人を第一に考えるグローバルバイオ企業であるインスメッドは、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指しています。当社は既承認薬から、中期から後期開発段階にある治験薬、最もニーズの高い患者コミュニティに提供する先進的な創薬まで、多様なポートフォリオを推進しています。インスメッドの最も進んだ段階にあるプログラムは、米国・日本・欧州で承認された慢性かつ消耗性の肺疾患の治療をはじめとする肺疾患と炎症性疾患に関するものです。当社の初期段階の研究プログラムは、遺伝子療法、AIを用いたタンパク質工学、タンパク質製造、RNA端末結合、合成レスキューなど、幅広い技術とモダリティを網羅しています。インスメッドは、米国ニュージャージー州ブリッジウォーターに本社を置き、欧州や日本において事業を展開しています。インスメッドはScience誌のトップエンプロイヤーサーベイで5年連続1位に選ばれ、バイオ医薬品産業で優良企業の1つとして認められています。
日本法人概要
会社名 : インスメッド合同会社
設立日 : 2017年12月5日
住所 : 〒100-0014 東京都千代田区永田町2-10-3 東急キャピトルタワー13階
https://insmed.jp/
Insmed®, Insmed logo, インスメッド®, ARIKAYCE® and アリケイス® are registered trademarks of Insmed Incorporated. PARI® is a registered trademark of PARI GmbH. Lamira® and ラミラ® are registered trademarks of PARI Pharma GmbH. All other trademarks referenced herein are the property of their respective owners.
将来予想に関する記述
本プレスリリースには、重大なリスクおよび不確定要素を伴う将来予想に関する記述が含まれております。1995年米国民事証券訴訟改革法に定義されているように「将来予想に関する記述」は、歴史的事実ではない記述であり、多くのリスクや不確定要素を伴っています。本プレスリリース記載の「かもしれない」、「予定する」、「はずである」、「可能性がある」、「だろう」、「期待する」、「計画する」、「見込む」、「信じる」、「見積もる」、「想定する」、「予測する」、「予定する」、「可能性がある」、「継続する」およびその他同様の表現(ならびに将来の事象、条件、状況に言及しているその他の言葉や表現)は、将来予想に関する記述であることを示しています。
本プレスリリースに記載されている将来予想に関する記述は、当社の現時点での予測や見解に基づくものであり、既知および未知のリスク、不確定要素およびその他の要因を伴っています。これらの要因により、当社の実際の業績、実績、成果および特定の事象の発生時期が、将来予想に関する記述で検討、予測、予想または提示されているそれらと大きく異なる可能性があることをご留意ください。これらのリスク、不確定要素およびその他要因には、以下のものが含まれます。当社が随時発表又は公表するENCORE試験を含む当社の臨床試験のトップラインデータが、より多くの患者データが利用可能になるにつれて変化したり、追加データが開示された場合に異なる解釈がなされたりするリスク。米国、欧州、もしくは日本での商業化を継続的に成功させられないこと、または ARIKAYCEに対する米国、欧州、もしくは日本の承認を維持できないこと。当社がFDAから ARIKAYCEの完全な承認 (full approval) を取得できないこと、または当社がARIKAYCEの適応症をより広範な患者集団に拡大するための規制当局の承認を取得できないこと。米国、欧州、および日本以外においてARIKAYCE に対する規制当局の承認(各市場および各用途での Lamira® Nebuliser Systemの個別の規制当局の承認を含む)を取得できないこと、または取得が遅れること。適用される規制当局の承認を得た場合でも、より広範な患者集団に対してARIKAYCEの商業化に成功しないこと。ARIKAYCEに対する、医師、患者、第三者支払者、および医療コミュニティのその他の者による市場受容度の不確実性または変化。ARIKAYCEのより広範な患者集団に対しての適応拡大が承認された場合でも、政府または第三者支払者から適切な償還を受けられないこと、または維持できないこと、または当社が許容可能な価格を得られないこと、または維持できないこと。 ARIKAYCEの潜在的市場規模の当社推定値の不正確性、または、医師、予想される患者導入率、予想される治療期間、または予想される患者の服薬遵守率もしくは中止率を特定するために用いたデータの不正確性。当社が製造を委託している第三者が、商業上の必要性に応じて十分な量の ARIKAYCEを製造できないこと、または当社の事業に影響を与える契約または法律および規制を遵守できないこと。当社が効果的な直接販売およびマーケティング基盤を構築もしくは維持できないこと、またはARIKAYCEを流通させるためのかかる基盤を提供する第三者と提携できないこと。 ARIKAYCEに関する予期せぬ安全性又は有効性の懸念の発現。当社とPARI社とのライセンス契約を含むARIKAYCEに関する契約により当社に課される制限、または当該契約にもとづく当社の義務の不履行。製造物責任請求を含む、当社が当事者であるか、または当事者となる可能性のある訴訟から生じる費用および潜在的評判の悪化。適切な規制当局によって承認された追加の第三者製造施設を建設する計画の実行の遅延、および、かかる計画に関連する予期しない費用。
将来予想に関する記述は、その性質上将来発生するまたは発生しない可能性のある事象に関連し、かつ将来発生するまたは発生しない可能性のある状況に依存するため、リスクおよび不確定要素を伴うことから、当社が将来予想に関する記述で示した実績、計画、意図、または予測を実際に達成できない場合があります。当社の事業に影響を及ぼすリスクや不確定要素に関する追加情報については、2025年12月31日を期末とするインスメッド年次報告書(Form 10-K)およびそれ以降に米国証券取引委員会(SEC)に提出している書類に記載されているItem 1A「リスク要因(Risk Factors)」で説明されている要因をご覧ください。
将来予想に関する記述は、あくまでも本プレスリリースの公表日現在における発表であるため、それらに過度に依拠することのないようご注意ください。当社は、法律および米国証券取引委員会(SEC)の規則で特に定められている場合を除き、予測の変化、かかる記述の根拠となる事象、条件、状況の変化、または実際の結果が将来予想に関する記述に記載されたものと異なる可能性に影響を与えうる変化を反映するために、かかる記述を公に更新または修正する義務を負いません。