ニュースリリースは報道関係者を対象とした、配信時当時の情報を掲載しています。
医療関係者や一般の方々を対象とした医学的な情報提供や、プロモーションを目的としたものではありません。
報道参考資料
本資料は、インスメッド(米国 ニュージャージー州)が2026年4月7日(現地時間)に発表したプレスリリースを日本語に翻訳編集したもので、その内容および解釈については、英語原文の記載及び米国における規制等に基づくものが優先されます。本資料は、報道関係者各位へ参考資料として提供するもので、医薬品のプロモーションや宣伝・広告を目的とするものではありません。英語版は、https://investor.insmed.com/2026-04-07-Insmed-Provides-Clinical-Update-on-Phase-2b-CEDAR-Studyをご参照ください。
インスメッド®、第IIb相CEDAR試験におけるアップデートを発表
- 本試験は主要評価項目および副次評価項目を達成せず、インスメッドはHSプログラムの開発を中止する。
- 安全性プロファイルはこれまでの試験結果と一貫しており、ブレンソカチブのいずれの用量においても新たな安全性シグナルは認められなかった。
2026年4月7日、米国ニュージャージー州発 人を第一に考え、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指すグローバルバイオ医薬品企業のインスメッド®(Nasdaq: INSM)は、本日、中等症から重症の化膿性汗腺炎(HS)を有する成人患者を対象にブレンソカチブを評価した第IIb相CEDAR試験において、10 mg群および40 mg群のいずれの投与群においても、主要評価項目および副次評価項目を達成しなかったことを発表しました。ブレンソカチブは良好な忍容性を示し、これまでにインスメッドが検討した中で最高用量である40 mg群を含め、いずれの用量においても新たな安全性シグナルは認められませんでした。インスメッドは、HSにおけるブレンソカチブの開発プログラムを中止するとともに、これらのデータを今後の学会で発表する予定です。
インスメッドの最高医学責任者(CMO)であるマルティナ・フラマー(M.D., M.B.A.)は、次のように述べています。「CEDAR試験は、確立された動物モデルが存在しないことから臨床開発が特に困難とされる疾患であるHSにおいて、ブレンソカチブが患者さんにベネフィットをもたらす可能性があるかどうかを検証するための概念実証試験(proof-of-concept試験)として設計されました。本試験結果については残念に思っておりますが、本試験から得られた知見がHSに関する科学的理解のさらなる深化に貢献することを期待しています。本試験にご参加いただいた患者さんおよび治験参加医師の皆様に、心より感謝申し上げます。」
本試験では16週時点において、ベースラインからの膿瘍および炎症性結節(AN)の総数がブレンソカチブ10 mg群および40 mg群ではそれぞれ45.5%および40.3%減少したのに対し、プラセボ群では57.1%の減少が認められました。16週間のプラセボ対照治療期間中における治験薬投与後に発現した有害事象(TEAE)の発現割合は以下のとおりです。
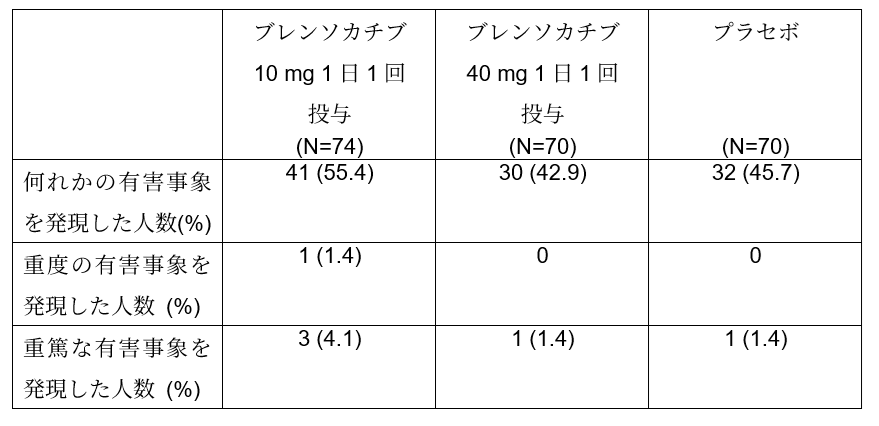
第IIb相CEDAR試験について
CEDAR試験は、中等症から重症の化膿性汗腺炎(HS)を有する成人患者を対象に、ブレンソカチブの有効性および安全性を評価するために実施された、無作為化、二重盲検、プラセボ対照の第IIb相試験です。本試験では、世界72施設において214名の患者が登録されました。本試験において、参加者はブレンソカチブ10 mg群、ブレンソカチブ40 mg群、またはプラセボ群に1:1:1の割合で無作為に割り付けられ、1日1回、16週間投与を受けました。最初の16週間終了後、参加者は無作為化時と同じ用量のブレンソカチブの投与を継続し、プラセボ群に割り付けられていた場合はブレンソカチブ10 mgまたは40 mgのいずれかに再度無作為に割り付けられました。主要評価項目は、16週時点における膿瘍および炎症性結節(AN)の総数のベースラインからの変化率でした。
インスメッドについて
人を第一に考えるグローバルバイオ企業であるインスメッドは、深刻な疾患と生きる患者さんの未来を変える、ファースト・イン・クラスおよびベスト・イン・クラスの治療法の実現を目指しています。当社は既承認薬から、中期から後期開発段階にある治験薬、最もニーズの高い患者コミュニティに提供する先進的な創薬まで、多様なポートフォリオを推進しています。インスメッドの最も進んだ段階にあるプログラムは、米国・日本・欧州で承認された慢性かつ消耗性の肺疾患の治療をはじめとする肺疾患と炎症性疾患に関するものです。当社の初期段階の研究プログラムは、遺伝子療法、AIを用いたタンパク質工学、タンパク質製造、RNA端末結合、合成レスキューなど、幅広い技術とモダリティを網羅しています。インスメッドは、米国ニュージャージー州ブリッジウォーターに本社を置き、欧州や日本において事業を展開しています。インスメッドはScience誌のトップエンプロイヤーサーベイで5年連続1位に選ばれ、バイオ医薬品産業で優良企業の1つとして認められています。
日本法人概要
会社名 : インスメッド合同会社
設立日 : 2017年12月5日
住所 : 〒100-0014 東京都千代田区永田町2-10-3 東急キャピトルタワー13階
https://insmed.jp/
Insmed®, Insmed logo, andインスメッド® are registered trademarks of Insmed Incorporated.
将来予想に関する記述
本プレスリリースには、重大なリスクおよび不確定要素を伴う将来予想に関する記述が含まれております。1995年米国民事証券訴訟改革法に定義されているように「将来予想に関する記述」は、歴史的事実ではない記述であり、多くのリスクや不確定要素を伴っています。本プレスリリース記載の「かもしれない」、「予定する」、「はずである」、「可能性がある」、「だろう」、「期待する」、「計画する」、「見込む」、「信じる」、「見積もる」、「想定する」、「予測する」、「予定する」、「可能性がある」、「継続する」およびその他同様の表現(ならびに将来の事象、条件、状況に言及しているその他の言葉や表現)は、将来予想に関する記述であることを示しています。
本プレスリリースに記載されている将来予想に関する記述は、当社の現時点での予測や見解に基づくものであり、既知および未知のリスク、不確定要素およびその他の要因を伴っています。これらの要因により、当社の実際の業績、実績、成果および特定の事象の発生時期が、将来予想に関する記述で検討、予測、予想または提示されているそれらと大きく異なる可能性があることをご留意ください。これらのリスク、不確定要素およびその他要因には、以下のものが含まれます。当社が随時公開もしくは公表する臨床試験からのトップラインデータ(CEDARスタディを含む)が、より多くの被験者のデータが入手できたことにより変化したり、もしくは追加データの取得により異なる解釈がされるリスク。当社が計画している将来の臨床試験が成功しないこと (当社が、試験を実施および完了するために、または規制当局の承認に必要なデータを得るために十分な数の患者を登録もしくは維持できない可能性があることを含む)。当社の製品候補に関連する安全性または有効性に関する予期しない懸念の発生。当社が当事者となる可能性のある訴訟(製造物責任請求を含む)から生じる費用および潜在的な評判の損失。
将来予想に関する記述は、その性質上将来発生するまたは発生しない可能性のある事象に関連し、かつ将来発生するまたは発生しない可能性のある状況に依存するため、リスクおよび不確定要素を伴うことから、当社が将来予想に関する記述で示した実績、計画、意図、または予測を実際に達成できない場合があります。当社の事業に影響を及ぼすリスクや不確定要素に関する追加情報については、2025年12月31日を期末とするインスメッド年次報告書(Form 10-K)およびそれ以降に米国証券取引委員会(SEC)に提出している書類に記載されているItem 1A「リスク要因(Risk Factors)」で説明されている要因をご覧ください。
将来予想に関する記述は、あくまでも本プレスリリースの公表日現在における発表であるため、それらに過度に依拠することのないようご注意ください。当社は、法律および米国証券取引委員会(SEC)の規則で特に定められている場合を除き、予測の変化、かかる記述の根拠となる事象、条件、状況の変化、または実際の結果が将来予想に関する記述に記載されたものと異なる可能性に影響を与えうる変化を反映するために、かかる記述を公に更新または修正する義務を負いません。